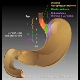
Magenkarzinom
Klinische Einteilung
Histologisch lassen sich folgende Karzinomtypen abgrenzen: Adenokarzinom (ca. 70%, papilläres, muzinöses, tubuläres Ca.) und das undifferenzierte Siegelringzellkarzinom (ca. 30 %). Makroskopisch lassen sich drei Typen des Magenkarzinoms unterscheiden: (1) das polypöse Karzinom, (2) das exulzerierend wachsende Karzinom und (3) das szirrhös wachsende Karzinom. Das Frühkarzinom (10 - 15 % bei Diagnosestellung) wird durch die Begrenzung des Tumorwachstums auf die Mukosa/Submukosa (T1) definiert, unabhängig vom Nachweis von Lymphknotenmetastasen. Helicobacter pylori ist ein wesentlicher Risikofaktor für das distale Magenkarzinom. Im Rahmen eines HNPCC besteht ein höheres Risiko für das Auftreten eines Magenkarzinoms.
Möglich ist eine Assoziation zwischen einer gastroösophagealen Refluxkrankheit (GERD) und der Entstehung eines Adenokarzinoms des Magens (AEG II und III).
Wichtig für die Festlegung des Resektionsausmaßes ist die histopathologische Einteilung nach Laurén in (1) den intestinalen Typ (gut differenziert) und den nicht-intestinalen Typ (diffus, schlecht differenziert). Tumoren des nicht-intestinalen Typs benötigen in der Regel (Ausnahme: Frühkarzinom; T1 N0) eine totale Gastrektomie mit Lymphadenektomie von Kompartment I, II und III.
Die Kardiakarzinome werden in drei Typen unterteilt (AEG I-III, siehe unter Ösophaguskarzinom), die für die Wahl des Operationsverfahrens hohe Relevanz haben.
Pathogenese, Ätiologie
- Exogene Noxen: wichtig vor allem beim intestinalen Typ: Multiple exogene Noxen; sozialer Status; Ernährung; Nikotin; C2H5OH;
- Endogene Noxen: unbekannt
Wichtige Risikofaktoren für das distale Magenkarzinom sind Alter, niedriger sozioökonomischer Status, Rauchen, übermäßiger Alkoholkonsum, vorangegangene Magenoperationen, perniziöse Anämie, familiäre Belastung, Leben in einer Hochrisikopopulation sowie Ernährungs- und Umweltfaktoren.
Präkanzerosen: Adenom; "borderline lesion" Perniziosa; M. Menetier; chronisch atrophische Gastritis; Z.n. distaler Magenresektion;
Epidemiologie
- Inzidenz: BRD: dritthäufigstes Karzinom beim Mann, zweithäufigstes Karzinom der Frau. Das "lifelong risk", am Karzinom zu erkranken, beträgt etwa 1:93 (1.07%) beim Mann und 1:152 (0.66%) bei der Frau (www.cancer.org)
- Altersgipfel 55-70 Jahre
- Geschlecht Männer > Frauen
- Geographie Gehäuftes Auftreten: Japan, Südosteuropa, Südamerika.
- Spontanverlauf ungünstig;
Metastasierung
| Leber | 57 % |
| Lunge | 28 % |
| Nebenniere | 22 % |
| Peritoneum | 15 % |
| Nieren | 8 % |
| Ovarien | 5 % |
| Skelett | 4 % |
TNM-Klassifikation 7. Auflage 2010
| TNM | Bemerkungen | |
| T 0 | Kein Anhalt für Primärtumor | |
| Tis | Carcinoma in situ | |
| T1 | Infiltration von Lamina propria oder der Tela submucosa | |
| T1a | Infiltration der Lamina propria oder der Lamina muscularis mucosae | |
| T1b | Infiltration der Tela submucosa | |
| T2 | Infiltration der Tunica muscularis | |
| T3 | Infiltration der Serosa (des viszeralen Peritoneums) | Infiltration des subserösen Bindegewebes ohne Invasion des viszeralen Peritoneums oder benachbarter Strukturen. T3 schließt auch Tumoren ein, welche sich entlang des gastrokolischen oder gastrohepatischen Ligaments ausbreiten, sowie das Omentum majus oder minus erreichen, ohne Durchdringung des viszeralen Peritoneums, welche diese Strukturen umgibt. |
| T4 | Infiltration von Nachbarstrukturen | Infiltration von Nachbarorganen |
| T4a | Infiltration der Serosa (viscerales Peritoneum) | |
| T4b | Infiltration von Nachbarorganen | |
| N0 | keine perigastrischen LK befallen | Regionäre Lymphadenektomie unter Mitnahme von 15 oder mehr Lymphknoten |
| N1 | LK-Metastasen in 1-2 lokalen LK | |
| N2 | LK-Metastasen in 3-6 lokalen Lymphknoten | |
| N3 | Metastasen in mehr als 7 lokalen LK | |
| N3a | 7-15 LK | |
| N3b | > 15 LK | |
| M0 | keine Fernmetastasen | |
| M1 | Fernmetastasen |
(*) Regionäre Lymphknotenmetastasen sind die perigastrischen LK entlang der kleinen und grosen Kurvatur, der A. gastrica sinistra, A. hepatica communis, A. coeliaca, der A. lienalis und der hepatoduodenalen Lymphknoten. Ein Befall von retropankreatischen, mesenterialen oder paraaortalen Lymphknoten gilt als Fernmetastasierung.
Stadieneinteilung des Magenkarzinoms nach UICC (2010)
| Stadium 0 | TIS | ||
| Stadium Ia | T1 | N0 | M0 |
| Stadium Ib | T1 | N1 | M0 |
| T2 | N0 | M0 | |
| Stadium IIa | T1 | N2 | M0 |
| T2 | N1 | M0 | |
| T3 | N0 | M0 | |
| Stadium IIb | T1 | N3 | M0 |
| T2 | N2 | M0 | |
| T3 | N1 | M0 | |
| T4a | N0 | M0 | |
| Stadium IIIa | T2 | N3 | M0 |
| T3 | N2 | M0 | |
| T4a | N1 | M0 | |
| Stadium IIIb | T3 | N3 | M0 |
| T4a | N2 | M0 | |
| T4b | N0,N1 | M0 | |
| Stadium IIIc | T4a | N3 | M0 |
| T4b | N2,N3 | M0 | |
| Stadium IV | Tx | Nx | M1 |
Prästationäre Maßnahmen (Hausarzt):
Basis-OP-Vorbereitung,
Obligate Diagnostik
Generell: Die Gewinnung einer Histologie ist dringlich. Bei "high-grade" intraepithelialen Neoplasien (früher Dysplasien) sollte eine externe pathologische Zweitbefundung durch einen erfahrenen Pathologen durchgeführt werden.
- Endoskopie und EUS (Endosonographie)
- Computertomographie des Abdomens und des Thorax mit i.v. Kontrast und Distension des Magens mit Kontrastmittel (Gastrografin) oder Wasser)
- Bei Adenokarzinomen des gastrointestinalen Übergangs kann ein PET-CT durchgeführt werden
- bei den anderen Karzinomen ist das PET-CT nicht erforderlich
- Thoraxübersicht
- B-Bild-Sonographie
- Risikoprofil: Basisdiagnostik + Kreatininclearance
 Digitalvideo: Endoskopie bei Magenantrumkarzinom
Digitalvideo: Endoskopie bei Magenantrumkarzinom
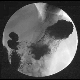 Abbildung: Gastrografinschluck bei Magenantrumkarzinom
Abbildung: Gastrografinschluck bei Magenantrumkarzinom
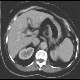 Abbildung: CT Abdomen mit Magenwandverdickung bei Magenkorpuskarzinom
Abbildung: CT Abdomen mit Magenwandverdickung bei Magenkorpuskarzinom
Fakultative Diagnostik
- Laparoskopie (Ausschluß Peritonealkarzinose, lokale Tumorausdehnung) bei cT3 oder cT4 Stadien
Hinweise
- Tumormarker müssen in der Primärdiagnostik keine mehr bestimmt werden. Molekulare Marker sind nur innerhalb klinischer Studien indiziert und in der klin. Routine nicht notwendig
Therapievorgehen [Chirurgie]
Aufklärung
Wundheilungsstörung, Anastomoseninsuffizienz, postoperativ Dysphagie und Gewichtsverlust, B12 Substitution lebenslang, Milzverletzung, Splenektomie, ggf. Pankreasresektion, Blutung, Reoperation, Fremdblut, Hepatitis, AIDS, Rezidiv, bei Komplikation Behandlung auf Intensivstation, Sepsis, Nachbeatmung, bei Langzeitbeatmung evtl. Luftröhrenschnitt
Vorbereitung
Legen eines zentralen Venenkatheters. Abführen mit 1/2-1 Portion Senna z.B. [X-Prep].
Bei Magenstumpfkarzinom: Kolonvorbereitung, da evtl. Querkolon reseziert werden muß.
Operationsverfahren
Standardlymphadenektomie:
Lymphadenektomie im Kompartment I und II (D2 Lymphadenektomie). Es wird angestrebt, > 25 regionäre Lymphknoten zu entfernen. Eine histopathologische Beurteilung "N0" ist nur bei Untersuchung von mind 16 LK gestattet.
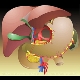 |
Kompartment I |
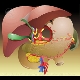 |
Kompartment II |
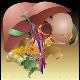 |
Lymphknotenstationen 12, 13 des Kompartment III |
- 1. Tag: Beginn der enteralen Sondenernährung
- 3. Tag.: Magensonde ex.
- 4. Tag: Schluckweise Tee, dann schrittweise Kostaufbau.
- 5. Tag: Robinson-Drainage ex.
Keine Routine-Kontrolle der Anastomose erforderlich. Lebenslange B12-Substitutionstherapie (3 monatlich. z.B. B12-Vicotrat im., iv., 1 Amp.). Ernährungsberatung. Pankreasfermentsubstitution sinnvoll (z.B. Kreon forte 3x2 o. 3x1 Kps., Btl. zu den Hauptmahlzeiten).
Therapieschemen [Innere/Endoskopie]
Oberflächliche Magenkarzinome, die auf die Mukosa begrenzt sind (T1a N0 M0), können unter Berücksichtigung folgender Kriterien mit einer endoskopischen Resektion behandelt werden (basierend auf der Japanischen Klassifikation der Magenkarzinome):
- Läsionen von < 2 cm Größe in erhabenen Typen
- Läsionen von < 1 cm Größe in flachen Typen
- Histologischer Differenzierungsgrad: gut oder mäßig (G1/G2)
- Keine makroskopische Ulzeration
- Invasion begrenzt auf die Mukosa
- Keine restliche invasive Erkrankung nach ER
Anzustreben ist eine en-bloc-Resektion
Therapieschemen [Onkologie]
Neoadjuvante Chemotherapie
Bei Patienten mit uT2 Stadium kann, ab uT3 Stadium soll eine neoadjuvante platinhaltige Chemotherapie durchgeführt werden.
Adjuvante Therapie: Nach präoperativer Chemotherapie und anschließender Operation sollte die Chemotherapie postoperativ fortgesetzt werden. Die Wirkung einer alleinigen adjuvanten Therapie ist nicht gesichert. Ausnahme: Eine adjuvante Radiochemotherapie kann bei einer Resektion ohne die geforderte D2-Lymphadenektomie diskutiert werden.
Additive Therapie: Bei R1 oder R2 Stadium (mikro- oder makroskopische Reste nach Resektion) soll zunächst über eine Nachresektion in ausgewiesenem Zentrum diskutiert werden. Ist diese nicht möglich oder sinnvoll, wird eine additive Radiochemotherapie empfohlen.
Alleinige Chemotherapie
Eine palliative Chemotherapie sollte bei ausreichendem Allgemeinzustand und nicht-resektablem Karzinom bzw. Lymphknoten- oder Leberfiliae angeboten werden. Vor dem Einsatz einer palliativen medikamentösen Tumortherapie sollte der HER-2-Status bestimmt werden (Therapie mit Trastuzumab) bestimmt werden.
Bei Bestrahlung der Milz oder Splenektomie akzidentell oder onkologisch: Impfungen !
Palliative Maßnahmen
Palliative Resektion zur Passagewiederherstellung, bei Tumorperforation oder Blutung. Alternativ: Anlage einer Gastroenterostomie (ggf. laparoskopisch);. Endoskopische Lasertherapie
Anhaltspunkte zur Prognose
Unbehandelt: infaust
Resezierte Patienten: Stadium I-IIIa ca. 60-70% 5J-ÜZ; Stadium IIIb-IV 20-0%
Prognostische Faktoren: R-Status nach chirurgischer Therapie, TNM-Kategorie, Lymphknotenquotient nach chirurgischer Therapie (Anzahl befallen / Anzahl entfernt), Komplikationsauftreten nach chirurgischer Therapie
Siehe auch: